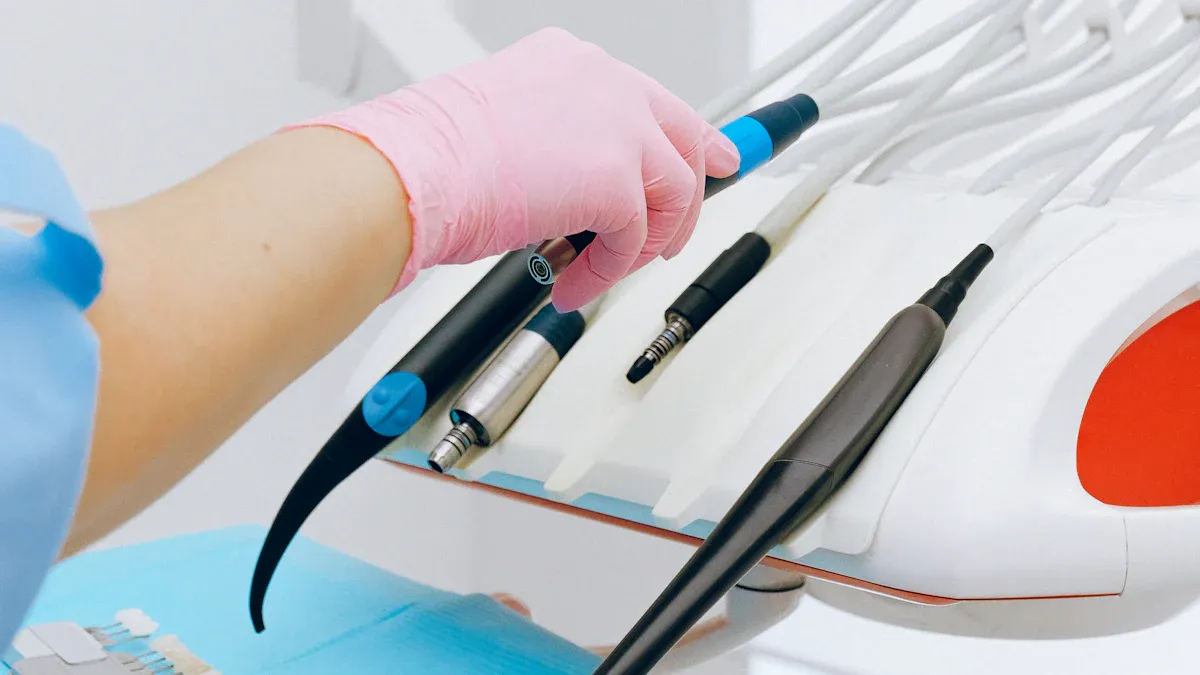
CE-zertifizierte kieferorthopädische Produkte spielen eine entscheidende Rolle in der modernen Zahnmedizin, indem sie Sicherheit und Qualität gewährleisten. Diese Produkte erfüllen strenge EU-Standards und garantieren somit ihre Zuverlässigkeit für Patienten und Behandler. Die EU-Medizinprodukteverordnung (MDR) hat strenge Anforderungen zur Erhöhung der Patientensicherheit eingeführt. Zum Beispiel:
- Zahnärztliche Instrumente müssen jetztrückverfolgbar bis zu ihrem Sterilisationsprozess.
- Zahnärzte, die CAD/CAM-Technologie einsetzen, unterliegen zusätzlichen Compliance-Pflichten, einschließlich Risikomanagementsystemen.
Die Einhaltung dieser Standards schützt die Patienten und gewährleistet, dass Zahnkliniken ihren gesetzlichen Verpflichtungen nachkommen, wodurch Vertrauen und Professionalität in diesem Bereich gefördert werden.
Wichtigste Erkenntnisse
- Die CE-Zertifizierung belegt, dass kieferorthopädische Produkte sicher und von hoher Qualität sind.
- Zahnkliniken sollten die Etiketten überprüfen und Dokumente anfordern, die die CE-Zertifizierung bestätigen.
- Regelmäßige Kontrollen helfen Kliniken, Probleme zu erkennen und die EU-Medizinprodukteverordnung (MDR) einzuhalten, um die Sicherheit der Patienten zu gewährleisten.
- Der Einkauf bei vertrauenswürdigen Lieferanten senkt die Risiken und verbessert die Patientenversorgung.
- Die Schulung der Mitarbeiter hinsichtlich der EU-MDR-Vorschriften trägt dazu bei, dass jeder weiß, wie man für Sicherheit und hohe Qualität sorgt.
Was sind CE-zertifizierte kieferorthopädische Produkte?
Definition und Zweck der CE-Zertifizierung
Die CE-Kennzeichnung ist ein in der gesamten Europäischen Union anerkanntes Qualitäts- und Sicherheitszeichen. Sie bestätigt, dass ein Produkt den EU-Vorschriften entspricht und somit die Standards für Gesundheit, Sicherheit und Umweltschutz erfüllt. Bei kieferorthopädischen Produkten garantiert diese Zertifizierung die Sicherheit für Patienten und die Wirksamkeit bei der vorgesehenen Anwendung. Zahnkliniken setzen auf CE-zertifizierte kieferorthopädische Produkte, um einen hohen Behandlungsstandard zu gewährleisten und das Vertrauen ihrer Patienten zu stärken.
Die CE-Kennzeichnung dient nicht nur der Einhaltung von Vorschriften. Sie fördert auch eine einheitliche Produktqualität auf dem EU-Markt. Dadurch wird sichergestellt, dass kieferorthopädische Produkte wie Brackets und Drähte unabhängig von ihrem Herstellungs- oder Anwendungsort zuverlässig funktionieren.
CE-Zertifizierungsverfahren für kieferorthopädische Produkte
Das CE-Zertifizierungsverfahren für kieferorthopädische Produkte umfasst mehrere wichtige Schritte. Hersteller müssen zunächstdie spezifischen Marktanforderungen verstehenDazu gehört auch die Notwendigkeit der CE-Kennzeichnung in der EU. Sie müssen außerdem sicherstellen, dass ihre Produkte die in der EU-Medizinprodukteverordnung (MDR) festgelegten grundlegenden Sicherheits- und Leistungskriterien erfüllen. Die Zusammenarbeit mit akkreditierten Prüfstellen ist für eine strenge Bewertung der Produktkonformität und -qualität unerlässlich.
Ein weiterer wichtiger Aspekt ist die regelmäßige Information über regulatorische Änderungen. Fachpublikationen und Rechtsexperten liefern wertvolle Einblicke in die Fristen für die Einhaltung der Vorschriften und die sich entwickelnden Standards. Sobald ein Produkt alle Prüfungen bestanden hat, erhält es die CE-Kennzeichnung und ist damit für den EU-Markt zugelassen.
Beispiele für CE-zertifizierte kieferorthopädische Produkte
CE-zertifizierte kieferorthopädische Produkte umfassen eine breite Palette an Instrumenten und Geräten für Zahnarztpraxen. Beispiele hierfür sind Brackets, Drahtbögen und Aligner. Diese Produkte werden strengen Tests unterzogen, um höchste Sicherheits- und Leistungsstandards zu gewährleisten. So werden beispielsweise Brackets von Herstellern wie Denrotary Medical mit modernster Ausrüstung gefertigt und unterliegen strengen Qualitätskontrollen. Dadurch können sich Zahnärzte auf diese Produkte verlassen und ihren Patienten effektive und sichere Behandlungen anbieten.
Die EU-MDR-Standards verstehen
Wichtigste Anforderungen der EU-Medizinprodukteverordnung für kieferorthopädische Produkte
Die EU-Medizinprodukteverordnung (MDR), offiziell bekannt alsEU 2017/745Diese Verordnung schafft einen umfassenden Rahmen für die Regulierung von Medizinprodukten, einschließlich kieferorthopädischer Produkte. Sie ist seit Mai 2021 in allen EU-Ländern verbindlich. Ziel ist es, die Sicherheit zu erhöhen, Innovationen zu fördern und eine gleichbleibende Qualität zu gewährleisten.
Zu den wichtigsten Anforderungen gehören:
- Keine BestandsschutzregelungGeräte, die gemäß der vorherigen Medizinprodukterichtlinie (MDD) zugelassen wurden, müssen neuen Konformitätsbewertungen unterzogen werden, um den MDR-Standards zu entsprechen.
- Eindeutige Geräte-Kennung (UDI)Alle kieferorthopädischen Produkte müssen eine UDI (Unique Device Individual) enthalten, um die Rückverfolgbarkeit zu verbessern.
- SterilisationskontrolleDentalinstrumente müssen die Rückverfolgbarkeit ihrer Sterilisationsprozesse nachweisen können.
Diese Anforderungen gewährleisten, dass kieferorthopädische Produkte strenge Sicherheits- und Leistungsstandards erfüllen und somit Patienten und Behandler gleichermaßen schützen.
Wie die EU-Medizinprodukteverordnung Sicherheit und Leistung gewährleistet
Die EU-Medizinprodukteverordnung (MDR) verbessert Sicherheit und Leistungsfähigkeit durch strenge regulatorische Maßnahmen. Hersteller müssen klinische Nachweise erbringen, um die Sicherheit und Wirksamkeit ihrer Produkte zu belegen. Dies umfasst die Dokumentation des gesamten Lebenszyklus eines Medizinprodukts.
Die Verordnung schreibt außerdem vor, dassQualitätsmanagementsystem (QMS)und ein System zur Überwachung nach dem Inverkehrbringen (Post-Market Surveillance, PMS). Diese Systeme überwachen die Produktleistung und gehen auf potenzielle Risiken ein. Beispielsweise müssen kieferorthopädische Produkte die Normen der ISO 14971:2019 für Risikomanagement erfüllen. Durch die Festlegung dieser Maßnahmen minimiert die EU-Medizinprodukteverordnung (MDR) die Wahrscheinlichkeit unerwünschter Ereignisse, wie sie in früheren Skandalen um Medizinprodukte aufgetreten sind.
Aktuelle Änderungen der EU-Medizinprodukteverordnung mit Auswirkungen auf Zahnkliniken
Mehrere Neuerungen der EU-Medizinprodukteverordnung (MDR) wirken sich direkt auf Zahnkliniken aus. Der Übergang von der Medizinprodukterichtlinie (MDD) zur MDR, der seit Mai 2021 gilt, erfordert, dass alle zuvor zugelassenen Medizinprodukte bis Mai 2024 neu bewertet werden. Dies gewährleistet die Einhaltung der neuesten Standards.
Die Einführung des UDI-Systems verbessert die Rückverfolgbarkeit von Produkten, insbesondere von implantierbaren Medizinprodukten der Klasse III. Darüber hinaus gelten Zahnärzte, die CAD/CAM-Technologie einsetzen, nun als Hersteller. Sie müssen Qualitätsmanagementsysteme implementieren und die Vorgaben der Medizinprodukteverordnung (MDR) erfüllen.
Die EUDAMED-Datenbank stellt eine weitere wichtige Neuerung dar. Diese Plattform sammelt und verarbeitet Informationen über Medizinprodukte und verbessert so Transparenz und Informationsfluss. Diese Änderungen unterstreichen die Bedeutung der Einhaltung der Vorschriften für Zahnkliniken, die CE-zertifizierte kieferorthopädische Produkte verwenden.
Warum die Einhaltung von Vorschriften für Zahnkliniken wichtig ist
Risiken der Nichteinhaltung der EU-MDR
Die Nichteinhaltung der EU-Medizinprodukteverordnung (MDR) birgt erhebliche Risiken für Zahnkliniken. Verstöße gegen die Vorschriften können schwerwiegende rechtliche Konsequenzen nach sich ziehen, darunter Bußgelder, Strafen oder sogar die Betriebsschließung. Kliniken riskieren zudem einen Reputationsschaden, der das Vertrauen der Patienten untergraben und den langfristigen Erfolg gefährden kann. Darüber hinaus erhöht die Verwendung nicht konformer kieferorthopädischer Produkte die Wahrscheinlichkeit von unerwünschten Ereignissen wie Geräteausfällen oder Patientenverletzungen, was kostspielige Gerichtsverfahren zur Folge haben kann.
Die Nichteinhaltung der EU-Medizinprodukteverordnung (MDR) kann den Klinikbetrieb beeinträchtigen. Beispielsweise kann das Fehlen einer eindeutigen Produktkennzeichnung (UDI) bei kieferorthopädischen Produkten die Rückverfolgbarkeit erschweren und somit die Bestandsverwaltung und die Patientenversorgung verkomplizieren. Kliniken, die es versäumen, ein Qualitätsmanagementsystem (QMS) oder ein System zur Marktüberwachung (PMS) einzuführen, haben möglicherweise Schwierigkeiten, Sicherheitsbedenken effektiv zu begegnen und setzen sich dadurch verstärkt der behördlichen Kontrolle aus.
Vorteile der Verwendung CE-zertifizierter kieferorthopädischer Produkte
Die Verwendung CE-zertifizierter kieferorthopädischer Produkte bietet Zahnkliniken zahlreiche Vorteile. Diese Produkte erfüllen strenge Sicherheits- und Leistungsstandards und gewährleisten so zuverlässige und effektive Behandlungen. Patienten profitieren von besseren Behandlungsergebnissen, während Kliniken einen guten Ruf für qualitativ hochwertige Versorgung erlangen. Die CE-Zertifizierung vereinfacht zudem die Einhaltung der EU-Medizinprodukteverordnung (MDR) und reduziert den Verwaltungsaufwand für Kliniken.
Kliniken, die CE-zertifizierte Produkte bevorzugen, können ihre Abläufe optimieren. Die Rückverfolgbarkeit dieser Produkte verbessert beispielsweise die Bestandsverwaltung und unterstützt die Sterilisationskontrolle. Dadurch wird sichergestellt, dass alle Instrumente den Hygienestandards entsprechen und das Infektionsrisiko minimiert wird. Darüber hinaus verfügen CE-zertifizierte Produkte häufig über eine umfassende Dokumentation, die es Kliniken erleichtert, die gesetzlichen Bestimmungen einzuhalten.
Rechtliche und ethische Verantwortlichkeiten von Zahnkliniken
Zahnkliniken haben sowohl rechtliche als auch ethische Verpflichtungen zur Einhaltung der EU-Medizinprodukteverordnung (MDR). Rechtlich müssen Kliniken sicherstellen, dass alle Medizinprodukte, einschließlich kieferorthopädischer Produkte, den regulatorischen Anforderungen entsprechen. Dies umfasstImplementierung interner KontrollenSie führen regelmäßige Audits durch und pflegen die technische Dokumentation. Kliniken müssen außerdem eine für die Einhaltung der regulatorischen Bestimmungen verantwortliche Person (PRRC) benennen, die die Einhaltung dieser Standards überwacht.
Aus ethischer Sicht müssen Kliniken der Patientensicherheit und der Vertraulichkeit höchste Priorität einräumen. Der Schutz der Patientendaten, insbesondere bei elektronischen Patientenakten, ist unerlässlich. Kliniken müssen zudem für alle Behandlungen eine informierte Einwilligung einholen und diese in klarer und verständlicher Sprache erläutern. Durch die Förderung einer Kultur der Integrität und Transparenz können Kliniken das Vertrauen ihrer Patienten gewinnen und zur Weiterentwicklung der Zahnmedizin beitragen.
Sicherstellung der Einhaltung der Vorschriften in Ihrer Zahnklinik
Schritte zur Überprüfung der CE-Zertifizierung von Produkten
Überprüfung derCE-ZertifizierungDie Einhaltung der EU-MDR-Vorschriften ist bei kieferorthopädischen Produkten unerlässlich. Zahnkliniken sollten daher zunächst die Produktkennzeichnung prüfen. Das CE-Zeichen muss deutlich sichtbar sein, ebenso wie die Kennnummer der benannten Stelle, die das Produkt bewertet hat. Kliniken sollten außerdem die Konformitätserklärung des Herstellers anfordern. Dieses Dokument bestätigt, dass das Produkt alle geltenden regulatorischen Anforderungen erfüllt.
Die Prüfung der technischen Dokumentation ist ein weiterer wichtiger Schritt. Jedes Produkt sollte über einen klinischen Bewertungsbericht (CER) und entsprechende Nachweise zur Sicherheit und Leistungsfähigkeit verfügen. Kliniken können zudem die EUDAMED-Datenbank konsultieren, um den Registrierungs- und Konformitätsstatus des Produkts zu überprüfen. Durch die regelmäßige Aktualisierung dieser Prüfungen wird sichergestellt, dass alle in der Klinik verwendeten kieferorthopädischen Produkte den geltenden Vorschriften entsprechen.
Auswahl seriöser Lieferanten für kieferorthopädische Produkte
Die Auswahl seriöser Lieferanten ist entscheidend für die Einhaltung hoher Standards in der zahnärztlichen Versorgung. Kliniken sollten Lieferanten bevorzugen, die die Branchenvorschriften einhalten, wie zum Beispiel:CE-Kennzeichnung in der EU oder FDA-Zulassung in den USAUnabhängige Prüfstellen spielen eine entscheidende Rolle bei der Überprüfung der Qualität und Konformität von Produkten. Kliniken sollten sich im Rahmen der Lieferantenauswahl nach diesen Zertifizierungen erkundigen.
Leistungskennzahlen (KPIs) helfen bei der Beurteilung der Zuverlässigkeit eines Lieferanten. Kennzahlen wie Ausbeute, Fertigungszykluszeit und Umrüstzeit geben Aufschluss über Produktionseffizienz und Flexibilität. Die Festlegung klarer Qualitätsstandards, wie beispielsweise der Fehlerrate nach Six Sigma oder des akzeptablen Qualitätsniveaus (AQL), gewährleistet eine gleichbleibende Produktqualität. Die Zusammenarbeit mit Lieferanten, die diese Kriterien erfüllen, reduziert Compliance-Risiken und erhöht die Patientensicherheit.
Schulung der Mitarbeiter zu den EU-MDR-Konformitätsanforderungen
Die Schulung der Mitarbeiter zur Einhaltung der EU-Medizinprodukteverordnung (MDR) ist ein proaktiver Weg, die Einhaltung der Vorschriften sicherzustellen. Kliniken sollten Workshops und Schulungen anbieten, um die Mitarbeiter über die neuesten MDR-Aktualisierungen zu informieren. Zu den Themen sollten die Bedeutung der CE-Kennzeichnung, die Rolle von eindeutigen Produktkennzeichnungen (UDI) und die Anforderungen an die Führung der technischen Dokumentation gehören.
Praxisnahe Schulungen verbessern das Verständnis der Mitarbeiter für die Compliance-Verfahren. So lernen sie beispielsweise, CE-Zertifizierungen zu überprüfen, die Rückverfolgbarkeit von Sterilisationsprozessen zu gewährleisten und Risikomanagementsysteme zu implementieren. Regelmäßige Schulungen steigern nicht nur die Kompetenz der Mitarbeiter, sondern fördern auch eine Compliance-Kultur in der Klinik.
Regelmäßige Compliance-Audits durchführen und Dokumentation
Regelmäßige Compliance-Audits spielen eine entscheidende Rolle, um sicherzustellen, dass Zahnkliniken die EU-Medizinprodukteverordnung (MDR) einhalten. Diese Audits helfen, Prozesslücken aufzudecken, Produktzertifizierungen zu überprüfen und zu gewährleisten, dass alle kieferorthopädischen Geräte den regulatorischen Anforderungen entsprechen. Kliniken, die routinemäßige Audits durchführen, können potenzielle Probleme proaktiv angehen, bevor diese zu rechtlichen oder sicherheitsrelevanten Risiken führen.
Um ein effektives Compliance-Audit durchzuführen, sollten Kliniken einem strukturierten Ansatz folgen:
- Erstellen Sie eine Prüfcheckliste: Berücksichtigen Sie wichtige Bereiche wie Produktzertifizierungen, Sterilisationsprotokolle und Schulungsnachweise des Personals.
- Technische Dokumentation prüfen: Stellen Sie sicher, dass für alle kieferorthopädischen Produkte aktuelle klinische Bewertungsberichte (CERs) und Konformitätserklärungen vorliegen.
- Inventar prüfen: Stellen Sie sicher, dass alle Geräte das CE-Zeichen tragen und die Rückverfolgbarkeitsanforderungen, wie z. B. die eindeutige Gerätekennung (UDI), erfüllen.
- Prozesse bewerten: Beurteilung der Sterilisationsverfahren, der Risikomanagementsysteme und der Aktivitäten zur Marktüberwachung.
Tipp: Es sollte ein Compliance-Beauftragter speziell für die Überwachung des Auditprozesses eingesetzt werden. Dies gewährleistet Verantwortlichkeit und Konsistenz bei der Einhaltung regulatorischer Standards.
Die Dokumentation ist für den Nachweis der Einhaltung der Vorschriften ebenso wichtig. Kliniken müssen detaillierte Aufzeichnungen über Audits führen, einschließlich der Ergebnisse, Korrekturmaßnahmen und Folgemaßnahmen. Diese Aufzeichnungen dienen als Nachweis bei Inspektionen durch die Aufsichtsbehörden. Sie helfen den Kliniken außerdem, ihre Fortschritte bei der Erfüllung der EU-Medizinprodukteverordnung (MDR) zu verfolgen.
Ein gut dokumentiertes Compliance-System gewährleistet nicht nur die Einhaltung gesetzlicher Bestimmungen, sondern schafft auch Vertrauen bei den Patienten. Kliniken, die Transparenz und Verantwortlichkeit priorisieren, erwerben sich einen Ruf für qualitativ hochwertige Versorgung. Durch die Integration regelmäßiger Audits und einer sorgfältigen Dokumentation in ihre Abläufe können Zahnkliniken die komplexen Anforderungen der EU-Medizinprodukteverordnung (MDR) souverän bewältigen.
CE-zertifizierte kieferorthopädische Produkte spielen eine entscheidende Rolle für die Patientensicherheit und die Einhaltung gesetzlicher Bestimmungen. Sie erfüllen die strengen EU-MDR-Standards, die die Qualität und Zuverlässigkeit der zahnärztlichen Versorgung gewährleisten. Durch die Einhaltung dieser Vorschriften können Zahnkliniken ihre Patienten schützen und das Vertrauen in ihre Leistungen stärken. Die Priorisierung der Compliance erfüllt nicht nur rechtliche Verpflichtungen, sondern beweist auch das Engagement für höchste Professionalität. Kliniken, die diese Praktiken anwenden, tragen zu sichereren und effektiveren kieferorthopädischen Behandlungen bei und setzen Maßstäbe für Qualität in der Branche.
Häufig gestellte Fragen
Was bedeutet das CE-Zeichen auf kieferorthopädischen Produkten?
DerCE-KennzeichnungDieses Siegel bestätigt, dass ein Produkt den EU-Sicherheits-, Gesundheits- und Umweltstandards entspricht. Es gibt Zahnkliniken und Patienten die Gewissheit, dass das Produkt strenge regulatorische Anforderungen erfüllt und wie vorgesehen funktioniert.
TippVor dem Kauf von kieferorthopädischen Produkten sollten Sie stets das CE-Zeichen und die dazugehörige Dokumentation überprüfen.
Wie können Zahnkliniken die Einhaltung der EU-Medizinprodukteverordnung (MDR) sicherstellen?
Zahnkliniken können die Einhaltung der Vorschriften sicherstellen, indem sie die CE-Zertifizierung überprüfen, ordnungsgemäße Dokumentation führen und regelmäßige Audits durchführen. Auch die Schulung des Personals zu den Anforderungen der EU-Medizinprodukteverordnung (MDR) und die Auswahl seriöser Lieferanten spielen eine entscheidende Rolle für die Erfüllung der regulatorischen Standards.
Sind CE-zertifizierte Produkte für Zahnkliniken in der EU obligatorisch?
Ja, CE-zertifizierte Produkte sind für Zahnkliniken in der EU obligatorisch. Diese Produkte erfüllen die strengen Sicherheits- und Leistungsstandards der EU-Medizinprodukteverordnung (MDR) und gewährleisten so die Patientensicherheit und die Einhaltung gesetzlicher Bestimmungen.
Was ist die eindeutige Geräte-Kennung (UDI) und warum ist sie wichtig?
Die UDI ist ein eindeutiger Code, der Medizinprodukten zur Rückverfolgbarkeit zugewiesen wird. Sie hilft Kliniken, Produkte während ihres gesamten Lebenszyklus zu verfolgen und so eine ordnungsgemäße Bestandsverwaltung und Patientensicherheit zu gewährleisten.
NotizDas UDI-System ist eine zentrale Anforderung der EU-Medizinprodukteverordnung (MDR).
Wie häufig sollten Zahnkliniken Compliance-Prüfungen durchführen?
Zahnkliniken sollten mindestens jährlich Compliance-Audits durchführen. Regelmäßige Audits helfen, Lücken aufzudecken, Produktzertifizierungen zu überprüfen und die Einhaltung der EU-Medizinprodukteverordnung (MDR) sicherzustellen. Häufige Überprüfungen minimieren Risiken und gewährleisten eine hohe Behandlungsqualität.
Emoji-Erinnerung:
Veröffentlichungsdatum: 29. März 2025


